Värme och temperatur Fysik1: Skillnad mellan sidversioner
Hakan (diskussion | bidrag) |
Hakan (diskussion | bidrag) Ingen redigeringssammanfattning |
||
| (14 mellanliggande sidversioner av samma användare visas inte) | |||
| Rad 4: | Rad 4: | ||
Vi mäter temperaturen när vatten kokas upp i vattenkokare. | Vi mäter temperaturen när vatten kokas upp i vattenkokare. | ||
[[Media:Koka_vatten_i_vattenkokare_12A.numbers | Mätdata vid kokning av vatten i vattenkokare]]. | |||
[[Fil:Doppvarmare.png|left]] | [[Fil:Doppvarmare.png|left]] | ||
| Rad 150: | Rad 152: | ||
=== Materialens egenskaper === | === Materialens egenskaper === | ||
Om du saknar formelsamling (men kan engelska bra) kan du använda Wolfram Alpha för att få reda på termiska egenskaper för material, exempelvis '''smältentalpitet''' (specific heat of fusion) och '''värmecapacitet''' (specific heat capacity). | |||
Skriv till exempel ''specific heat of fusion Water'' i på wolfram alpha.com. | |||
{{uppgruta|'''Hemuppgift''' | {{uppgruta|'''Hemuppgift''' | ||
| Rad 171: | Rad 173: | ||
Här är en GeoGebra som du kan använda till att räkna ut värmeenergin om c, m och T är kända. Självklart kan du skriva in andra värden på m, c och T. Du kan också öppna filen och göra egna formeler. Det fungerar ungefär som Excel. | Här är en GeoGebra som du kan använda till att räkna ut värmeenergin om c, m och T är kända. Självklart kan du skriva in andra värden på m, c och T. Du kan också öppna filen och göra egna formeler. Det fungerar ungefär som Excel. | ||
=== Använd | === Använd kalkylark för att lösa värmeuppgifter === | ||
Här under finns ett kalkylark där du kan beräkna värmeenergin för fyra olika ämnen genom att mata in massa och temperaturerna. temperaturskillnaden beräknaas automatiskt. Om du lägger in formel på någona annan av variablerna kan du även räkan ut denna. Det ganska användbart men det är miniräknaren ller Wolfram|Alpha också. | Här under finns ett kalkylark där du kan beräkna värmeenergin för fyra olika ämnen genom att mata in massa och temperaturerna. temperaturskillnaden beräknaas automatiskt. Om du lägger in formel på någona annan av variablerna kan du även räkan ut denna. Det ganska användbart men det är miniräknaren ller Wolfram|Alpha också. | ||
Här fanns en gång en GGB-applet. | |||
<br> | <br> | ||
| Rad 196: | Rad 198: | ||
<br> | <br> | ||
Här fanns en gång en GGB-applet. | |||
<br> | <br> | ||
=== Smältvärme === | === Smältvärme === | ||
| Rad 290: | Rad 292: | ||
{{uppgruta|'''Problemlösingsstrategi''' | {{uppgruta|'''Problemlösingsstrategi''' | ||
Lös någon uppgift med hjälp av en mall som ska träna dig i att använda en säker problemlösningsstrategi: [[Mall för att lösa fysikproblem]] | Lös någon uppgift med hjälp av en mall som ska träna dig i att använda en säker problemlösningsstrategi: [[Mall för att lösa fysikproblem]] | ||
}} | |||
== Verkningsgrad == | |||
{{uppgruta | '''Rätta labben''' | |||
Här finns en labbrapport där eleven fick hemuppgiften att beräkna verkningsgraden för kokning av vatten på spisen och med vattenkokare. Laborationen är bra genomförd men det finns allvarliga fel i beräkningarna. Din uppgift är att hitta felen och korrigera dem samt redovisa en godkänd rapport. | |||
: [[media: Fysik1_labb_t_dahlgren_u_kommentarer_men_lämplig_uppgift_att_finna_felen.pdf | Laborationsrapport med brister - Verkningsgrad vid vattenkokning]] | |||
Om du har gjort förbättringarna av rapporten kan du se mina kommentarer och jämföra med dina korrigeringar. | |||
: [[Media: Fysik1_labb_t_dahlgren_m_kommentarer.pdf | Laborationsrapport med kommentarer - Verkningsgrad vid vattenkokning]] | |||
}} | }} | ||
| Rad 402: | Rad 417: | ||
Själva provet finns att printa nedan samt en Powerpoint med exempel på lösningar. Vi diskuterar först lösningarnas kvaliteter och hur man kan betygsätta respektive uppgift. Därefter sättter ni betyg på uppgiften i ert prov. Ni gör sedan en samlad bedömning av betyget på provet. Jag godkänner sedan er egen bedömning. | Själva provet finns att printa nedan samt en Powerpoint med exempel på lösningar. Vi diskuterar först lösningarnas kvaliteter och hur man kan betygsätta respektive uppgift. Därefter sättter ni betyg på uppgiften i ert prov. Ni gör sedan en samlad bedömning av betyget på provet. Jag godkänner sedan er egen bedömning. | ||
{{print|[ | {{print| | ||
[[Media:Värme,_Fysik_1,_version2_2.pdf|Prov Fysik 1, Värme, version 2]]}} | |||
[http://wikiskola.se/images/Prov_Fysik_1_Värme_version_2_Facit.pptx Facit till provet Fysik 1 Värme version 2] | [http://wikiskola.se/images/Prov_Fysik_1_Värme_version_2_Facit.pptx Facit till provet Fysik 1 Värme version 2] | ||
Nuvarande version från 7 augusti 2017 kl. 18.20
Introlabb
Vi mäter resistans och beräknar effekten på doppvärmare och vattenkokare.
Vi mäter temperaturen när vatten kokas upp i vattenkokare.
Mätdata vid kokning av vatten i vattenkokare.

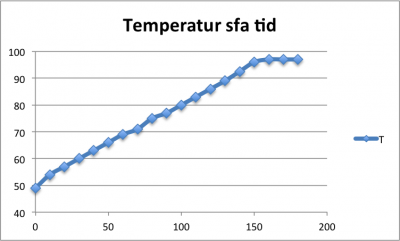
Ett samband mellan energi och temperatur.
Mätningarna ovan visar att när vattenkokaren sätts på så värms vattnet.
Den elektriska effekten blir alltså värme.
Uppvärmningen leder till en temperaturökning.
- [math]\displaystyle{ W = P t }[/math]
- [math]\displaystyle{ W \backsim \Delta T }[/math]
Värmeenergi
Ett närliggande begrepp är termisk energi, vilket är löst definierat som den energi hos en kropp som ökar med dess temperatur. Värme är den process där termisk energi flödar från ett system till ett annat.
Termisk energi är den inre energin i ett system som påverkas av temperaturen.
Temperatur
Kelvin (K) är SI-enheten för temperatur, uppkallad efter William Thomson, 1:e baron Kelvin. 1 K definieras som 1/273,16 av temperaturen vid vattens trippelpunkt (vilket motsvarar en temperatur av 0,01 °C och ett tryck av 611,73 Pa). Kelvinskalans nollpunkt är den absoluta nollpunkten. Enheten kelvin är vanligast förekommande i tekniska och vetenskapliga sammanhang. Celsiusskalan har kalibrerats så att mätvärden i grader Celsius är exakt 273,15 mindre än motsvarande mätvärden i kelvin. Skalstegen är exakt lika stora; en ökning i temperaturen med 1 kelvin är samma sak som en ökning med 1 °C. Sambandet mellan de två skalorna lyder:
- T[K] = T[°C] + 273,15
- T[°C] = T[K] − 273,15
Termodynamikens huvudsatser
Inom tekniken behandlar området värmeöverföring den energitransport som sker mellan system. Värmeöverföring leder till en förändring hos systemens termiska energi vilket kan ske till följd av masstransport, värmeledning, konvektion eller termisk strålning.
Termodynamikens nollte huvudsats
Värme, eller värmemängd, är ett begrepp inom termodynamiken som beskriver den energiöverföring som sker mellan två system till följd av en temperaturdifferens, vilket postuleras i termodynamikens nollte huvudsats. Värme kan även ses som den energiöverföring som sker till en system men som inte är i form av arbete.
Termodynamikens första huvudsats
Termodynamikens första huvudsats postulerar att differensen mellan tillfört värme (Q) och uträttat arbete (W) i ett system är lika stor som förändringen i systemets inre energi (U):
- [math]\displaystyle{ \Delta U = Q - W \ }[/math]
Termodynamikens andra huvudsats
Värmeöverföringen är en form av energiöverföring, värmeenergi.
Naturlig värmeöverföring sker endast spontant till den kallare kroppen, i enlighet med termodynamikens andra huvudsats. Värmeöverföringen till en kropp med samma eller högre temperatur kan endast ske med hjälp av en värmepump via mekaniskt arbete eller med speglar och linser som fokuserar den elektromagnetiska värmestrålningen och därmed ökar dess flödestäthet.
| Definition |
|---|
| Enkel formulering
Om det är en temperaturskillnad mellan två kroppar flödar värme från den varmare till den kallare kroppen. |
| Definition |
|---|
| Två mer vetenskapliga formuleringar
Värme kan inte av sig själv gå över från en kropp vid lägre temperatur till en annan med högre temperatur.
Det finns ingen process vars enda resultat är att värme från en enda värmekälla helt omvandlas till mekaniskt arbete.
|
Att spontana processer enbart sker i en riktning är ett välkänt faktum; exempelvis svalnar en kopp varmt kaffe i rumstemperatur, men samma kopp kaffe blir aldrig varm igen bara av att stå i rumstemperatur. Detta går inte att bevisa teoretiskt. Liksom i fråga om energiprincipen är det praktisk erfarenhet som har föranlett andra huvudsatsen. Texten och citaten ovan från Wikipedia
Entropi
Ju lägre entropin är, desto mer av värmet går således att omsätta i arbete - ju högre entropi, desto mer värme måste nödvändigtvis förloras och kan omöjligen omsättas i arbete. Till praktiskt arbetesutbyte odugliga (låggradiga, lågvärdiga) värmeflöden kännetecknas således av hög entropi medan det mekaniska arbetet i sig och därmed besläktade energislag som elektricitet och kemiskt bunden energi representeras av entropi lika med (eller mycket nära) noll.
med hjälp av en värmepump kan man med hjälp av mekaniskt arbete lyfta värmen till en högre temperatur. Idealt skulle man med en värmepump och den mängd mekaniskt arbete som gick att utvinna i en ideal värmemotor kunna återföra all värme till ursprungstemperaturen. I praktiken finns dock förluster och även om någon energi aldrig går förlorad kommer entropin oundvikligen ständigt att öka i ett system som innehåller både värmemotor och värmepump. Den sammansatta processen innehåller således ett irreversibelt moment - entropiförlust (= ökning av entropin) - som gör att ursprungstillståndet inte helt och hållet kan återställas. Entropin kan följaktligen också ses som karaktäriserande för graden av oordning hos tillståndet.
Termodynamikens tredje huvudsats
Minskad temperatur innebär minskad rörelse hos molekylerna.
Vid den absoluta nollpunkten (0 K) upphör all rörelse och alla processer.
Övning - mäta temperatur
| Uppgift |
|---|
| Snabblabb - Värmekapacitet
Gör ett eneklt experiment och bestäm värmekapaciteten för vatten Material: Doppvärmare, termos, vatten, mätglas, termometer (termoelement), stativ, klämma, muff. Kommentar Beroende på hur man löser omrörningen så borde man få ett värde +- 1000. |
| Uppgift |
|---|
| Alternativ snabblabb
Vi börjar med att blanda vatten av olika temperatur för att försöka komma fram till ett ssmband mellan värme och temperatur. |
Uppvärmning och avkylning
Specifik värmekapacitet
W = c m ∆T där ∆T 0 temperaturskillnaden, m = massan och c = specifika värmekapaciteten. Ibland skriver man cp där p anger att det är uppmätt vid konstant tryck. Enheten för c är kJ/(kg·K)
Eftersom det är en temperaturskillnad spelar det ingen roll om temperaturerna anges i Celsius eller Kelvin. Det blir däremot fel om man mot förmodan anger temperaturskillnaden i Fahrenheit. Varför det?
Tabell över specifika värmekapaciteten för några ämnen
Detta är värdena för metallerna i fast form. observera att värmekapaciteten skiljer sig mellan vatten och is (som är vatten i fast form).
| Ämne | Cp [kJ/(kg·K)] | |
|---|---|---|
| Järn | 0,449 | |
| Aluminium | 0,897 | |
| Vatten | 4,181 | |
| Is | 2,2 | |
| Silver | 0,24 | |
| Etanol | 2,44 | |
| Glas | 0,84 | |
| Paraffin | 2,1-2,9 | |
| Trä | 0,4 | |
| Luft | 1,00 |
Tabellen ovan från Wikipedia
Materialens egenskaper
Om du saknar formelsamling (men kan engelska bra) kan du använda Wolfram Alpha för att få reda på termiska egenskaper för material, exempelvis smältentalpitet (specific heat of fusion) och värmecapacitet (specific heat capacity).
Skriv till exempel specific heat of fusion Water i på wolfram alpha.com.
| Uppgift |
|---|
| Hemuppgift
A. Min vattenkokare hemma är märkt med effekten 1520 Watt. Det tar x s att värma 0.5 l 22-gradigt vatten till kokning. Vad har den för verkningsgrad. B. Gå hem och undersök verkningsgraden hos en vattenkokare eller mikrovågsugn på samma sätt. Det ingår i uppgiften att klura ut ett enkelt sätt att mäta vattnets temperatur. Lösning till A finns på diskussionssidan. |
Film
Tio minuters förklaring av Kamal Wafi:
Här är en GeoGebra som du kan använda till att räkna ut värmeenergin om c, m och T är kända. Självklart kan du skriva in andra värden på m, c och T. Du kan också öppna filen och göra egna formeler. Det fungerar ungefär som Excel.
Använd kalkylark för att lösa värmeuppgifter
Här under finns ett kalkylark där du kan beräkna värmeenergin för fyra olika ämnen genom att mata in massa och temperaturerna. temperaturskillnaden beräknaas automatiskt. Om du lägger in formel på någona annan av variablerna kan du även räkan ut denna. Det ganska användbart men det är miniräknaren ller Wolfram|Alpha också.
Här fanns en gång en GGB-applet.
Räkneuppgift - Fritidshuset
Faser och fasövergångar
Länk: latent heat
Tänkbar uppgift är att flippa över till den svenska motsvarande sidan och utöka denna. Klicka på svenska i vänsterspalten.
Nu ska det inte bara handla om att värma saker. Ibland behöver man räkna på vad som händer vid fasövergångarna. nedan ser du ett diagram där is värmts från -20 C. Sedan har isen smält vattnet värmt och sedan förångats.
Här fanns en gång en GGB-applet.
Smältvärme

Experimentet med is som smälter hade ett termoelement infruset i en klump is om cirka 1,5 dl storlek. Isklumpen placerades i en kastrull som stod på en värmeplatta. Värmeplattans effekt sattes på trean. Termoelementet är kopplat till en multimeter och mäter temperaturskillnaden mellan mätpunkten och en referenspunkt inne i mätinstrumentet. Detta ger upphov till ett systemeatiskt fel även om termoelementet mäter relativt exakta temperaturförändringar. I denna mätning ligger tmperatuerna cirka 2 grader för högt. Det vet vi ju eftersom vi börjar mäta i is.
Man ser av grafen att isen smälter utan att öka i temperatur. Smältvattnet har dock ökat i temperatur under det att isen smält därför ser vi en snabb ökning av den uppmätta temperaturen när termoelementet kommer ut ur isen och hamnar i det varma vattnet.
Därefter ser vi en någorlunda jämn ökning av vattnets temperatur under inverkan av tillförd värme från värmeplattan.
Detta enkla experiment visar två av de viktiga sambanden inom värmeläran och den nya formeln lyder så här:
- [math]\displaystyle{ E = c_s m }[/math]
Som så ofta är fallet använder olika författare olika beteckningar på storheter och konstanter. Läromedlet Nexus Fysik skriver formeln för smältvärme på följande sätt:
- [math]\displaystyle{ W_s = l_s m }[/math]
Ångbildningsvärme

- [math]\displaystyle{ E = c_k m }[/math]
eller Wå = låm som nexus skulle skrivit.
Experiment med ångbildningsvärme
Doppvärmare märkt 300 W.
- [math]\displaystyle{ P = \frac {W} {t} }[/math]
- [math]\displaystyle{ W = Pt (1) }[/math]
- [math]\displaystyle{ t = 4 min = 240 s. }[/math]
- [math]\displaystyle{ m_f_o_r_e = 300 ml = 0.3 kg }[/math]
- [math]\displaystyle{ m_{efter} = 270 ml = 0.27 kg }[/math]
Massan på det förångade vattnet = 0.300-0.270 = 0.030 kg
W = lå*m <==> lå = W/m lå = Pt/m om man använder (1)
lå = 300*240/0.03 = 2400 kJ/kg
Tabellvärdeet är 2260 kJ/kg
Felkällor: Mätningen av vattnets volym är inte vidare exakt. Vidare har vi gjort antagandet att all värme från doppvärmaren går till att förånga vattnet men viss värme strålar säkert i luften eller leds bort av termosen.
Uppgift: Antag att vi har gjort bra mätningar ovan men att inte 100% av effekten går in i förångningen. Vilekn verkningsgrad har vi då från doppvärmaren i vattnet?
Verkningsgraden = Peffektiv/Pdoppvärmare = Weffektiv/Wdoppvärmare = lå,tabell*m/lå,experiment*m = 2260/2400 = 94 %
Övrigt
Tabell över smältentalpitet och ångbildningsentalpitet
| Ämne | ls [kJ/kg] | lå [kJ/kg] | |
|---|---|---|---|
| Etanol | 105 | 841 | |
| Glykol | - | 800 | |
| Vatten | 334 | 2260 | |
| Metanol | - | 1100 |
Kamal Wafi förklarar uppvärmning och fasövergångar
Kamal Wafi räknar på uppvärmning av ett ämne
| Uppgift |
|---|
| Räkneövning - de tre värmeformlerna |
Det är bra att ha en fungerande metod när man löser problem och gör beräkningar. Här kommer en upgpift där du övar detta och får med dig en mall för att lösa framtida uppgifter.
| Uppgift |
|---|
| Problemlösingsstrategi
Lös någon uppgift med hjälp av en mall som ska träna dig i att använda en säker problemlösningsstrategi: Mall för att lösa fysikproblem |
Verkningsgrad
| Uppgift |
|---|
| Rätta labben
Här finns en labbrapport där eleven fick hemuppgiften att beräkna verkningsgraden för kokning av vatten på spisen och med vattenkokare. Laborationen är bra genomförd men det finns allvarliga fel i beräkningarna. Din uppgift är att hitta felen och korrigera dem samt redovisa en godkänd rapport. Om du har gjort förbättringarna av rapporten kan du se mina kommentarer och jämföra med dina korrigeringar. |
Praktisk räkneövningvning TE11
Bestäm verkningsgraden för mikro och vattenkokare genom att räkna baklänges
bestäm sedan ångbildningsentalpin.
Bestäm effekt in från värmeplattan genom att räkna baklänges. Bestäm ångbildningsentalpin.
Värmeöverföring samt Kylmaskiner och värmemotorer

Överkurs
Här är mallen för att lösa fysikproblem som ni använde på lektionen
Dela ut labbinstruktion till värmelabben.
Värmeöverföring
Det finns tre typer av värmeöverföring:
- strömning, exempelvis luften i ett rum eller vätskan i en kastrull.
- ledning i metaller och andra material.
- strålning, exempelvis från en eld, ugn eller solen.
Demo: Visa gärna värmeöverföring med metallstavar och provrör.
Film om värmeöverföring
Komprimering av en gas
Komprimering av en gas innebär att ett arbete uträttas, dvs energi tillförs och trycket ökar. Komprimeringen gör att volymen minskar. Detta leder till att temperaturen ökar enligt allmänna gaslagen. Tänk på en cykelpump. Den blir varm när luften i den komprimeras.
[math]\displaystyle{ pV = nRT }[/math]
Kompressionen i sig innebär att volymen minskar och trycket ökar. Det tillförda arbetet innebär att temperaturen ökar.
- Adiabatisk process
- Carnot-cykeln. Steg 3 och 4 i Carnotcykeln motsvara pumpens hoptryckning av gasen. Isotermisk kompression (där arbetet ger ett värmeflöde) följt av isentropisk kompression då temperaturen ökar. Enklare uttryckt: Arbetet på gasen blir värme samtidigt som en kompression.
Mikroexperiment: Andas ut på din hand. Hur känns det? Blås på handen. Hur känns det nu? Att det blir kallare när man blåser beror på att luften är under tryck i munnen men sedan minskar trycket utanför munnen varvid temperaturen sjunker.
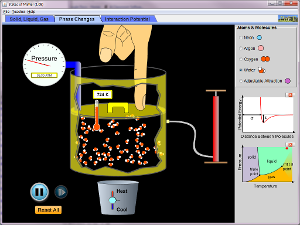
Lärarinstruktion till simuleringen nedan.
Om du trycker ned locket ökar temperaturen först och sedan ökar trycket. Jämför ideala gaslagen.
Kylning
Länkar:
Kylskåpets funktion
Man kan förklara hur kylskåpet fungerar genom att titta på hur gasen komprimeras och expanderar. Kompressorn komprimerar (pressar ihop) gasen utanför kylskåpet. Det höjer temperaturen på gasen men sedan går gasen i ringlande rör på baksidan av kylskåpet och kyls av. Sedan går gasen igenom en strypventil som håller trycket mot kompressorn. Men efter strypventilen lättar trycket och gasen expanderar i det rör som går in i kylskåpet. När gasen expanderar kyls den av och kan därför ta emot värme från kylskåpet som blir kallare. Även här går gasen i ringlande rör och den blir varmare mot slutet. Röret går ut ur kylskåpet igen och kommer till kompressorn som suger in gasen och pumpar upp den i tryck i gen på andra sidan. Så ser cykeln ut och den upprepas så fort kylskåpet behöver kylas.
Länkar
- Läs om Baltzar von Platen
- Finsk teve om kylskåpets funktion. Denna film har härlig finlandssvenska och förklarar kylskåptes funktion utifrån fasövergångar, alltså förångning och kondensation.
Värmemotorn och Carnotprocessen
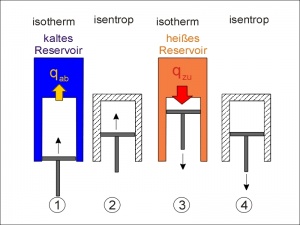
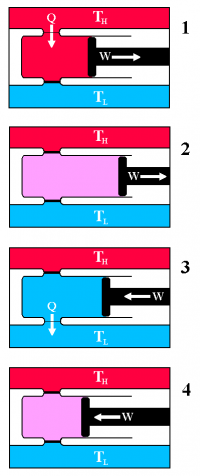
Wa = Wvarm - Wkall
Verkningsgrad för värmemaskiner
Härledning:
η = Wnyttig/Wtillförd = Wa/Wvarm = (Wvarm - Wkall)/Wvarm = 1 - Wkall/Wvarm = 1 - Tkall/Tvarm
Repetition
Tisdag v 5 och fredag v 5
Titta på Lars kylskåp utan skåp
Räkna
- Värmeuppgifter som övar formelhantering. Facit finner du som söker ett primtal större än 1896.
- Räkna A- och B-uppgifter, sid 148-149
- Fundera och diskutera, Prova själv och Varför har elefanter så stora öron?, sid 150-153
- Övningsprov Värme Fysik A
- Prov Värme version 1 (Gammalt prov från FysikA
- Facit till prov värme version 1 Endast svar.
- Lösningar till uppgift 5 och 9 i Värmeprovet.
- Beräkning till uppg 9 på provet
Facit till provet som PPT
Själva provet finns att printa nedan samt en Powerpoint med exempel på lösningar. Vi diskuterar först lösningarnas kvaliteter och hur man kan betygsätta respektive uppgift. Därefter sättter ni betyg på uppgiften i ert prov. Ni gör sedan en samlad bedömning av betyget på provet. Jag godkänner sedan er egen bedömning.